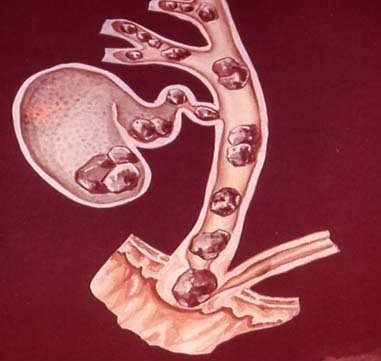
Острый лимфобластный лейкоз
Содержание:
Этиопатогенез
Точные причины возникновения ОЛЛ неизвестны. Предполагают, что, как и в случае других злокачественных заболеваний, болезнь развивается в результате неблагоприятного сочетания воздействия окружающей среды, наследственной предрасположенности и шанса. Изучение этиологии ОЛЛ усложняется разнообразием подтипов болезни, каждый из которых может иметь свои причины.
Возникновение злокачественного клона
Считают, что в случае детского В-ОЛЛ предлейкозный клон возникает в организме ребёнка ещё в ходе внутриутробного развития. При В-ОЛЛ, ассоциированном с мутацией гена MLL, злокачественное перерождение B-клетки, по всей видимости, завершается до рождения. Это подтверждается тем, что если он возникает у одного из монозиготных близнецов с общей или монохориональной плацентой, то возникает и у второго с вероятностью практически 100 % и проявляется вскоре после рождения. Пик заболеваемости В-ОЛЛ с другими цитогенетическими характеристиками приходится на более поздний возраст — 2—5 лет. Эти виды лейкоза развиваются у обоих близнецов только в 10—15 % случаев. Это может говорить о том, что, хотя предлейкозный клон возникает во время внутриутробного развития, для его окончательной трансформации нужны дополнительные события.
Возможные причины и факторы риска
В качестве возможных причин ОЛЛ рассматривают:
- ионизирующую радиацию — ионизирующая радиация была выявлена как причина ОЛЛ и других видов лейкоза при изучении последствий атомных бомбардировок Японии. Повышенная частота развития ОЛЛ была обнаружена у людей, работавших с радиографическим оборудованием до установления современного уровня безопасности. Люди, прошедшие курс радиотерапии, имеют повышенный риск развития так называемых вторичных лейкозов, в том числе и ОЛЛ. Рентгеновская пельвиметрия во время беременности немного увеличивает риск развития ОЛЛ у ребёнка, при этом риск растёт пропорционально числу процедур. Некоторые исследователи предполагают, что естественная радиация и космическое излучение могут быть причинами ОЛЛ, но эта точка зрения является спорной;
- инфекции — возбудитель детского ОЛЛ до сих пор не был обнаружен. Существует несколько гипотез на этот счёт, но они сходятся в том, что развитие лейкоза является результатом аномального иммунного ответа на присутствие инфекционного агента. По гипотезе Кинлена, причиной детского ОЛЛ является неизвестный возбудитель, скорее всего вирус, к которому у большинства детей развивается естественный иммунитет, однако у небольшой части особенно чувствительных детей этот возбудитель вызывает лейкоз. По гипотезе Гривса, причиной детского ОЛЛ может быть множество неспецифических возбудителей (например, вирусы гриппа), которые вызывают спонтанные мутации в B-клетках детей, имевших мало контактов с патогенами на первом—втором годах жизни (например, не посещавших ясли);
- генетическую предрасположенность — мутации, вызывающие ОЛЛ с высокой пенетрантностью, пока не обнаружены. Однако широкомасштабные исследования генома заболевших выявили, что некоторые аллельные варианты генов IKZF1, ARID5B, CEBPE и CDKN2A ассоциированы с повышенным риском развития ОЛЛ. Такие аллели имеют аддитивный эффект. Продукты перечисленных генов вовлечены в дифференцировку и пролиферацию кровяных клеток. Также риск развития ОЛЛ резко повышен у больных синдромом Дауна — примерно в 40 раз у детей в возрасте до четырёх лет.
Стадии патологии
В онкологической практике острый лейкоз делится на следующие стадии:
- Первая фаза имеет скрытое течение. В костном мозге зарождается злокачественный процесс, падает или поднимается уровень лейкоцитов. Формируются бласты.
- При развернутом этапе болезнь проявляется классическими симптомами. Процесс кроветворения нарушен. Инфекции активно поражают организм. Анализ крови определяет патологическое состояние.
- Рак крови проходит временно или полностью. Во время полной ремиссии восстанавливается уровень кровяных телец. Прекращаются мутации в кроветворном органе. Если болезнь отступает не полностью, на фоне хорошего самочувствия лимфоидный орган содержит повышенное количество бластов.
- Вторичный рак или рецидив характеризуется повторным поражением костного мозга или развитием новообразования в другом органе.
- На терминальной стадии незрелые лейкоциты распространяются по всем тканям и органам. Угнетаются функции систем человеческого тела. Лечение не приносит результатов. Присутствует постоянная угроза жизни пациента.
Диагностика
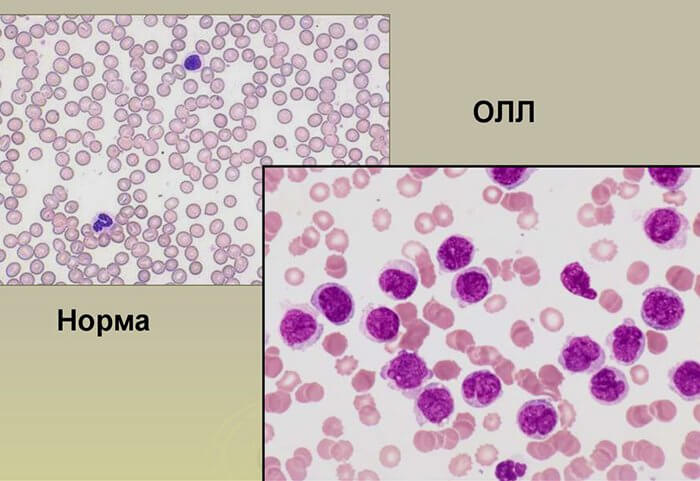
При ОЛЛ возникают изменения в обычном клиническом анализе крови: понижены уровни эритроцитов и тромбоцитов, появляются бластные клетки. Очень высокий лейкоцитоз возможен, но, вопреки распространенному мнению, наблюдается не во всех случаях. В целом же надежно поставить диагноз можно только при исследовании образца костного мозга; для этой цели необходима костномозговая пункция.
При морфологическом исследовании диагноз «острый лимфобластный лейкоз» ставится при обнаружении более 25% бластных клеток в костном мозге (в противном случае речь может идти о лимфобластной лимфоме). Но обязательно производятся более тонкие исследования: цитохимическое (окрашивание клеток, позволяющее более точно установить их природу), цитогенетическое (изучение строения хромосом в лейкемических клетках), иммунофенотипирование (изучение белковых молекул на поверхности клеток)
Дело в том, что при диагностике очень важно не только надежно отличить ОЛЛ от острого миелоидного лейкоза, но и определить конкретный вариант ОЛЛ, поскольку он сильно влияет на терапию и прогноз заболевания
Так, ОЛЛ может быть B-клеточным (около 80% случаев) и T-клеточным, в зависимости от того, относятся ли лейкемические клетки к B- или T-лимфоцитарной линии
В зависимости от «степени зрелости» бластных клеток среди как В-, так и Т-клеточных лейкозов выделяют несколько вариантов; их установление в ходе иммунофенотипирования важно для определения стратегии лечения. Все большую важность для определения терапии приобретают и генетические особенности опухолевых клеток
В ходе диагностики ОЛЛ также необходимо исследовать состояние центральной нервной системы. Анализ спинномозговой жидкости (ликвора) позволяет определить, нет ли у больного поражения центральной нервной системы – нейролейкемии. Образец ликвора для анализа получают посредством пункции спинномозгового канала.
Возможны и дополнительные диагностические процедуры для исследования пораженных лимфоузлов и внутренних органов – компьютерная томография (КТ), ультразвуковое исследование (УЗИ) и так далее.
Диагностические исследования позволяют для каждого конкретного больного определить ту или иную группу риска, от которой зависят прогноз заболевания и планируемое лечение. Так, говорят о стандартном риске, высоком риске и т.д. Отнесение к той или иной группе зависит от многих факторов. Перечислим некоторые из них.
- Возраст больного: менее благоприятным считается возраст до 1 года или старше 10 лет.
- Количество лейкоцитов: риск увеличивается при очень высоком лейкоцитозе в момент диагноза.
- Т-клеточный ОЛЛ у детей традиционно считается связанным с несколько более высоким риском по сравнению с В-клеточным.
- Хромосомные аномалии в лейкемических клетках, связанные с числом хромосом и транслокациями. При некоторых из них усложняется лечение болезни. Так, филадельфийская хромосома – транслокация t(9;22) – требует подключения дополнительных таргетных лекарств к терапии. Транслокация t(4;11) часто требует трансплантации костного мозга. В то же время, например, транслокация t(12;21) чаще всего связана с относительно хорошим прогнозом.
- Распространение ОЛЛ в другие органы, помимо костного мозга (например, возникновение нейролейкемии), определяет более высокий риск.
- При раннем или повторном рецидиве лейкоза риск значительно повышается.
Лечение хроническоголимфолейкоза
| Препарат | Механизм действия | Способ применения | Эффективность |
| Флударабин | Цитостатический препарат из группы пуриновых аналогов | 25 мг/м2 внутривенно в течение трёх дней. Интервал между курсами – один месяц | Считается наиболее эффективным пуриновым аналогом. Полные ремиссии удаётся получить у большинства пациентов. Для продления периода ремиссии рекомендуется применение данного препарата в сочетании с другими цитостатиками |
| Циклофосфамид | Противоопухолевое, цитостатическое, иммунодепрессивное, алкилирующее действие | 250 мг/м2 внутривенно в течение трёх дней | В сочетании с другими препаратами составляет наиболее эффективные схемы лечения с наименьшим количество побочных эффектов |
| Ритуксимаб | Моноклональные антитела к антигену CD20 | 375 мг/м2раз в три недели | В сочетании с цитостатиками повышает вероятность достижения полных и длительных ремиссий |
| Хлорамбуцил | Алкилирующее вещество, блокатор синтеза ДНК | От 2 до 10 мг в сутки в течение 4-6 недель | Считается эффективным цитостатиком с избирательным действием на лимфоидную опухолевую ткань |
- «FCR» — флударабин, циклофосфамид, ритуксимаб – самая распространённая и высокоэффективная схема лечения;
- Хлорамбуцил+ритуксимаб – применяется при наличии соматических патологий;
- «СОР» — циклофосфамид, винкристин, преднизолон – программа повторяется каждые 3 недели, проводится в общем 6-8 циклов, назначается обычно при прогрессировании заболевания на фоне лечения другими препаратами;
- «СНОР» — циклофосфамид, винкристин, преднизолон, адриабластин – проводится при отсутствии эффективности программы «СОР».
Лучевая терапияУдаление селезёнки
Лечение острого лимфобластного лейкоза
Врач определит оптимальный метод лечения ОЛЛ. Лечение проводится в два этапа. Первый этап — индукционная терапия, чтобы убить лейкозные клетки. Затем применяется поддерживающая терапия, чтобы уничтожить оставшиеся клетки лейкемии. Оставшиеся лейкозные клетки могут вызывать рецидивы. Лечение включает:
Химиотерапия
Химиотерапия — использование лекарственных препаратов для уничтожения раковых клеток. Лечение включает таблетки, инъекции и введение препаратов через катетер. Лекарства поступают в кровоток и разносятся по организму, убивая главным образом раковые, а также некоторые здоровые клетки.
В настоящее время проходят клинические испытания различные препараты, напримет препарат иматиниба (Гливек). Этот препарат используется для лечения хронического миелолейкоза (ХМЛ). Гливек помогает предотвратить изменение функции генов, связанных с ОЛЛ.
Некоторые типы ОЛЛ могут распространиться на головной и спинной мозг. В этом случае может быть использована интратекальная химиотерапия. Препараты химиотерапии вводятся непосредственно в позвоночный столб.
Лучевая терапия
Лучевая терапия — использование радиоактивного излучения, чтобы убить раковые клетки и уменьшить опухоль. При ОЛЛ используется внешняя лучевая терапия. Опухоль облучается источником радиации, расположенным вне тела. Этот вид лечения используется для видов ОЛЛ, которые распространились или могут распространиться на головной и спинной мозг.
Химиотерапия с трансплантацией стволовых клеток
Химиотерапия сопровождается трансплантацией стволовых клеток (незрелые клетки крови). Они заменяют кроветворные клетки, разрушенные в результате лечения рака. Стволовые клетки отбираются из крови или костного мозга пациента или донора. Затем они вливаются в пациента.
Биологическая терапия
Этот метод лечения ОЛЛ все еще проходит испытания в клинических условиях. Лечение заключается в применении лекарств или веществ, которые используются для увеличения или восстановления естественной защиты организма от рака. Этот тип терапии также называется лечение с использованием модификаторов биологических реакций. Иногда используются очень специфические (моноклональные) антитела, разработанные для подавления лейкозных клеток. В настоящее время терапия с помощью моноклональных антител ограничена клиническими испытаниями и недоступна в России.
Причины возникновения острой лимфобластной лейкемии у взрослых
Как уже было сказано ранее, ОЛЛ у взрослых пациентов в большинстве случаев развивается на фоне возникновения и лечения других онкологических заболеваний. Его развитие провоцируют, в частности, препараты-цитостатики, входящие в протоколы всех видов химиотерапии, а также лучевая терапия.
Кроме того, причинами старта острого лейкоза лимфобластного типа может выступать наследственный фактор – образование так называемого злокачественного клона, представляющего собой группу клеток с неконтролируемым процессом размножения. Высока вероятность того, что клон образуется еще во внутриутробном периоде. Для того, чтобы такие клетки начали активно делиться, необходимо влияние внешних факторов, в частности:
- ионизирующее (радиоактивное) излучение;
- избыточное воздействие ультрафиолета;
- длительный систематический контакт с различными токсическими веществами, промышленными и пищевыми канцерогенами, пестицидами и гербицидами;
- наличие генетических заболеваний. Чаще, чем здоровые взрослые, острым лимфобластным лейкозом болеют пациенты с синдромами Дауна, Швахмана, Вискотта-Олдриджа, Клайнфельтера, а также анемией Фанкони, целиакией, нейрофиброматозом.
В некоторых медицинских источниках частоту возникновения ОЛЛ у взрослых связывают с курением и вирусными заболеваниями. Однако убедительной доказательной базы по этим гипотезам на сегодняшний день не существует.
Диагностика
Для постановки диагноза и определения типа заболевания требуются лабораторные исследования.
-
Общий анализ крови с подсчетом лейкоцитарной формулы для первичной диагностики патологии.
-
Биохимический анализ крови, чтобы выявить ухудшения в работе печени и почек.
-
Биопсия костного мозга для последующего изучения (обычно берется из подвздошной кости).
-
Гистологическое исследование биоптата. Необходимо для выявления злокачественных клеток.
-
Цитохимический анализ биоптата. Определяются специфические ферменты, характерные для тех или иных бластов.
-
Иммунофенотипический анализ. Определение поверхностных антигенов позволяет точно установить вид острого лейкоза.
-
Цитогенетический анализ. Выявляет повреждения хромосом, что позволяет точно определить разновидность заболевания.
-
Молекулярно-генетический анализ. Проводится в случаях, когда другие методы не дают однозначного результата.
-
УЗИ органов брюшины. Подтверждение увеличения размеров печени и селезенки, выявление метастазов в лимфоузлах и других внутренних органах.
-
Рентген грудной клетки. Выявление увеличенных лимфоузлов, воспалительного процесса в легких.
В дальнейшем могут понадобиться другие диагностические исследования для уточнения диагноза и для наблюдения за изменением состояния пациента.
Внимание!
Вы можете бесплатно получить медицинскую помощь в АО «Медицина» (клиника академика Ройтберга) по программе по программе Государственных гарантий ОМС (Обязательного медицинского страхования) и ВМП (высокотехнологичной медицинской помощи).
Чтобы узнать подробности, позвоните, пожалуйста, по телефону +7 (495) 775-73-60 , или можете прочитать более подробно здесь…
Причины
На гистологическом уровне, причиной развития острого лимфобластного лейкоза является бесконтрольное размножение групп клеток. В медицине данные клетки называют злокачественным клоном. Образуются они из-за хромосомных мутаций. Ученые предполагают, что еще во внутриутробном развитии ребенка закладывается генетическая предрасположенность к лимфобластному лейкозу. После рождения, при наличии внешних факторов, возможно провоцирование образования данного заболевания.
Специалисты связывают образование ОЛЛ со следующими факторами:
- лимфобластный лейкоз может спровоцировать применение лучевой терапии по борьбе с другими видами онкопроцессов, которыми страдал человек. Вероятность образования ОЛЛ после применения радиотерапии составляет около 10%. 85% пациентов заболевают острым лимфобластным лейкозом в течение 10 лет после окончания данного вида терапии;
- есть предположение, что частое использование рентгенологических исследований приводит к данной патологии. Но эта теория пока находится на уровне предположений;
- инфекционный характер образования лимфобластных лейкозов также пока остается на уровне гипотезы;
- перенесенные инфекционные заболевания матерью во время беременности, а также непосредственный контакт с ядовитыми химическими веществами могут спровоцировать лимфобластный лейкоз у ребенка в дальнейшем;
- при наличии у ребенка болезней, связанных с генетическими отклонениями (синдромы Дауна, Швахмана, Клайнфельтера, Вискотта-Олдрича);
- если ребенок рождается с избыточным весом, то считается, что у него есть предрасположенность к развитию ОЛЛ;
- предполагается, что злоупотребление вредными привычками, особенно табакокурением, могут стать толчком к образованию лимфобластных лейкозов.
Лечится ли?
При лечении лейкемии прогноз зависит от множества факторов – от формы и характера течения болезни, сроков обнаружения, степени поражения внутренних органов, общего состояния организма. Наименее благоприятны перспективы лечения взрослых пациентов старше 60 лет и детей старше 10 лет, особенно при наличии усложняющих факторов. В целом заболевание достаточно хорошо поддается терапии современными средствами, в число которых входят:
- химиотерапия;
- лучевая терапия;
- гемосорбция;
- таргетная терапия;
- трансплантация костного мозга или донорских стволовых клеток.
При своевременном начале лечения в специализированной онкогематологической клинике прогноз достаточно благоприятен, и врачам в большинстве случаев удается добиться длительной ремиссии либо полностью избавить пациента от заболевания.
Диагностика Лейкоза у детей:
При подозрении на лейкоз ребенка должен исследовать педиатр, а потом детский онкогематолог. Основной диагностики являются лабораторные методы: исследование периферической крови и костного мозга.
При остром лейкозе у ребенка выявляют в общем анализе крови типичные изменения:
— тромбоцитопения
— анемия
— высокая СОЭ
— ретикулоцитопени
— бластемия
— лейкоцитоз различной степени или лейкопения
— исчезновение базофилов и эозинофилов
Типичным признаком служит так называемый феномен «лейкемического провала»: между зрелыми и бластными клетками нет промежуточных форм.
Лейкоз диагностируют обязательно с проведением стернальной пункции и миелограммы. О болезни говорит содержание бластных клеток 30% и более. Если исследования костного мозга не дали четких результатов, ребенку делают трепанобиопсию. Чтобы определить вариант острого лейкоза, проводят такие исследования: иммунологические, цитохимические, цитогенетические.
Подтверждение диагноза проводится при участии детского офтальмолога и детского невролога. Также проводится в некоторых случаях рентгенография черепа, люмбальная пункция и исследование цереброспинальной жидкости, офтальмоскопия.
Вспомогательные методы диагностики лейкоза у детей:
- УЗИ слюнных желез
- УЗИ лимфоузлов
- УЗИ мошонки у мальчиков
- УЗИ печени и селезенки
- компьютерная томография у детей
- рентгенография органов грудной клетки
Лейкоз при диагностике врачи отличаются от лейкозоподобной реакции, которая бывает при коклюше, тяжелых формах туберкулеза, цитомегаловирусной инфекции, инфекционном мононуклеозе, сепсисе. При таких заболеваниях проявления лейкоза могут иметь обратимый характер.
Как установить стадию лейкоза?
Лейкозы стадируются не так, как большинство случаев рака. С самого начала болезни поражена периферическая кровь и костный мозг. Нужно выявить проникновение клеток лейкоза в селезенку, печень, лимфоузлы, ЦНС, яички, яичники.
Если в центральной нервной системе лейкозные клетки есть в большом количестве, то их фиксируют при помощи исследования спинномозговой жидкости под микроскопом. Если клетки выявлены, ребенку нужно более интенсивное лечение.
Прогностические факторы при лейкозе (лейкемии) у детей:
- Возраст на момент обнаружения болезни
- Возраст больного и исходное количество лейкоцитов
- Пол
- Количество лейкоцитов
- Раса
- Количество хромосом
- Иммунофенотипирование лейкозных клеток
- Ответ на лечение
- Хромосомные транслокации
Профилактика Острого лимфобластарного лейкоза:
Профилактика
Дозу 24 Гр на голову дают на 3 недели по 1,5 Гр за сеанс с двух латеральных полей.
Одну из двух инъекций метотрексата, вводимого 2 раза в неделю в спинномозговой канал, во время облучения головы целесообразно производить в субботу, так как в этот день, как правило, не бывает лучевой терапии, другую — в один из первых дней недели
после сеанса облучения головы; в день эндолюмбального введения метотрексата больной остается в стационаре.
В период профилактики нейролейкемии с помощью как облучения, так и введения метотрексата и цитозара, больные получают внутрь 6-меркаптопурин ежедневно в дозе 25 мг/м2 и циклофосфамид в дозе 100 мг/м2 1 раз в неделю.
После окончания профилактики нейролейкемии делают пункцию костного мозга, и если признаков рецидива нет, то начинают поддерживающую терапию.
Вторым методом профилактики нейролейкемии является эндолюмбальное введение метотрексата и цитозара. Препараты вводят с интервалом 3-4 дня, при плохой переносимости 1 раз в неделю.
Оба метода профилактики нейролейкемии надежны и позволяют отказаться от поддерживающих интралюмбальных введений метотрексата.
Непрерывное поддерживающее лечение в период улучшения острых лимфобластного и недифференцируемого лейкозов детей проводится амбулаторно, в течение 5 лет до полного улучшения. Начинают лечение сразу после достижения полного улучшения или после курсов, закрепляющих достигнутое улучшение.
Дети получают непрерывное лечение тремя препаратами по следующей схеме: 6-меркаптопурин внутрь ежедневно; метотрексат внутрь на 6-й день недели; циклофосфамид внутрь на 7-й день недели, в эти дни 6-меркаптопурин не отменяют.
Для «группы риска» в период непрерывного поддерживающего лечения тремя препаратами каждые 1,5-2 месяца проводится курс СО АР. Во время данного курса в течение недели после него поддерживающее лечение тремя препаратами отменяется, а затем в течение недели проводится половинными дозами. После этого поддерживающее лечение проводится полными дозами.
Условия проведения непрерывного лечения:
1) анализ крови с определением тромбоцитов и ретикулоцитов 1 раз в неделю;
2) при снижении уровня лейкоцитов до 1 Ч 103 — 2 Ч 103 (1000-2000) в 1 мкл врач снижает дозу цитостатических препаратов вдвое, при последующем его повышении более 2,5 Ч 103 (2500) в 1 мкл восстанавливают прежнюю дозу;
3) лечение прерывают на любом этапе при падении уровня лейкоцитов в крови ниже 1000 в 1 мкл, при значительном повышении температуры, стоматите, диарее;
4) пункцию костного мозга в первый год улучшения производят 1 раз в месяц; на 2-5-м году улучшения — 1 раз в 3 месяца.
Лечение острого лимфобластного лейкоза усиливается, когда речь идет о процессе Т-клеточной природы. По программе американских педиатров-онкологов для устранения проявлений болезни при Т-лимфобластном остром лейкозе начинают с внутривенного введения циклофосфана по 1200 мг/м2 в 1-й день лечения или между 2-м и 5-м днем (при уровне лейкоцитов более 5 Ч 104 (50 000) в 1 мкл и значительной органомегалии, требующих предварительного назначения аллопуринола из-за высокого уровня мочевой кислоты в сыворотке и опасности развития мочекислого диатеза). С 3-4-го дня (или в 1-й день, если введение циклофосфана отсрочено) еженедельно (1 раз в неделю) по этой программе, как и по программе Aur, вводится винкристин в течение 4 недели, а также
применяют преднизолон и рубомицин в дозах и в сроки, соответствующие схеме 2 лечения острого лимфобластного лейкоза.
При достижении ремиссии проводится курс ее консолидации, включающий 5-дневное непрерывное введение цитозара по 100 мг/(м2/сут.), прием тиогуанина (или 6-меркаптопурина) по 50 мг/м2 каждые 12 ч в течение 5 дней введения цитозара. Проводят 3 курса лечения цитозаром и тиогуанином (6-меркаптопурин) с интервалом между курсами 14 дней.
Затем в течение 7-14 дней внутривенно капельно вводят L-acnapaгиназу по 200-300 ЕД/кг. В случае высокого уровня лейкоцитов и большой массы опухолевых лимфатических узлов спленомегалии или гепатомегалии терапию нужно проводить, назначая больному большое количество жидкости, щелочное питье, наряду с аллопуринолом для профилактики мочекислого диатеза.
Если при Т-клеточном остром лейкозе в средостении определяются увеличенные лимфатические узлы, плохо сокращающиеся от химиотерапии, то рекомендуется локальное облучение этой области в дозе 30 Гр; локальное облучение целесообразно и при значительном увеличении лимфатических узлов любой другой области.
Лечение в период улучшения при Т-клеточном лейкозе должно быть усилено: наряду с непрерывной терапией 6-меркаптопурином, метотрексатом, циклофосфаном.
Причины и факторы риска
Непосредственной причиной заболевания всегда становится злокачественная мутация клеток кроветворной системы, из-за которой они становятся способны к быстрому бесконтрольному размножению. Существует предположение, что изменение генома происходит еще во время внутриутробного развития, но до определенного момента процесс остается незавершенным. «Спусковым крючком» нередко становятся внешние обстоятельства:
- радиоактивное излучение любой природы, в том числе во время лечения других форм рака;
- некоторые химические соединения – бензол, определенные препараты химиотерапии;
- вирусные инфекции (Эпштейна-Барр, HTLV);
- унаследованная предрасположенность.
Острый лимфоцитарный лейкоз часто развивается у детей, реже – у людей старше 60 лет, совсем редко – у взрослых. Представители белой расы заболевают чаще темнокожих, мужчины – несколько чаще женщин.
Симптомы Острого лимфобластного лейкоза:
Различают два типа течения острого лимфобластного лейкоза: В-линейный и Т-линейный, в зависимости от типа клеток — лимфоидных предшественников.
Все лейкоциты в организме человека делятся на 2 типа — гранулоцитарные и агранулоцитарные (зернистые и незернистые), эти две группы, в свою очередь, подразделяются на эозинофилы, базофилы, нейтрофилы (гранулоцитарные), и лимфоциты (В- и Т-типа) и моноциты (агранулоцитарные). В процессе созревания и развития (дифференцировки) все клетки проходят несколько этапов, первым из которых является бластный этап (лимфобласты). Из-за поражения костного мозга опухолью, лимфоциты не успевают достаточно развиться для того, чтобы полноценно исполнять свои защитные функции. По большей части, при остром лимфобластном лейкозе поражаются В-лимфоциты (примерно в 85% случаев), отвечающие за образование антител в организме.
Клинические признаки острого лимфобластного лейкоза
- Синдром интоксикации — слабость, лихорадка, недомогание, потеря веса. Лихорадка может быть связана и с наличием бактериальной, вирусной, грибковой или протозойной (реже) инфекцией, особенно у детей с нейтропенией (менее 1500 нейтрофилов в 1 мкл).
- Гиперпластический синдром — увеличение всех групп периферических лимфоузлов. Инфильтрация печени и селезенки приводит к их увеличению, что может проявляться болями в животе. Могут появиться боль и ломота в костях из-за лейкемической инфильтрации надкостницы и суставной капсулы и опухолевого увеличения объема костного мозга. При этом на рентгенограммах можно обнаружить характерные для лейкемической инфильтрации изменения, особенно в трубчатых костях, возле крупных суставов.
- Анемический синдром — бледность, слабость, тахикардия, кровоточивость слизистых полости рта, геморрагический синдром на коже, бледность. Слабость возникает в результате анемии и интоксикации.
- Геморрагический синдром связан как с тромбоцитопенией, так и с внутрисосудистым тромбозом (особенно при гиперлейкоцитозе) и приводит к появлению петехий, экхимозов на коже и слизистых, кровоизлияниям, мелене, рвоте с кровью.
- У мальчиков может обнаруживаться инициальное увеличение яичек ( 5-30% случаев первичного ОЛЛ). Это безболезненные, плотные, одно- или двусторонние инфильтраты. Особенно часто это бывает при гиперлейкоцитозе и Т-клеточном варианте ОЛЛ.
- Дыхательные нарушения, связанные с увеличение лимфоузлов средостения, которые могут привести к дыхательной недостаточности. Этот признак характерен для Т-линейного ОЛЛ.
- Могут появиться кровоизлияния в сетчатку глаза, отек зрительного нерва. При офтальмоскопии могут обнаруживаться лейкемические бляшки на глазном дне.
- Из-за сильно сниженного иммунитета любое повреждение кожи является очагом инфекции, могут появиться паронихии, панариции, инфицированные укусы насекомых и следы инъекций.
Достаточно редкими осложнениями могут являться поражения почек в результате инфильтрации (клинические проявления могут и отсутствовать) и выпотной перикардит из-за нарушения лимфооттока между эндокардом и эпикардом.
Признаки и симптомы острого лимфобластного лейкоза
ОЛЛ характеризуется множеством различных признаков и у разных больных может проявляться совершенно по-разному. Большинство наблюдаемых симптомов, однако, обусловлено тяжелыми нарушениями кроветворения: избыток аномальных бластных клеток при ОЛЛ сочетается с недостаточным количеством нормальных функциональных клеток крови.
Обычно наблюдаются слабость, бледность, снижение аппетита, потеря веса, учащенное сердцебиение (тахикардия) – проявления анемии и опухолевой интоксикации. Недостаток тромбоцитов проявляется мелкими кровоизлияниями на коже и слизистых оболочках, кровотечениями из десен, носовыми и кишечными кровотечениями, кровоподтеками, синяками. Из-за накопления бластных клеток часто увеличиваются лимфоузлы – в частности, шейные, подмышечные, паховые. Нередко увеличиваются также печень и селезенка — как говорят, возникает гепатоспленомегалия.
Часто наблюдаются боли в костях и суставах, иногда возникают патологические (то есть вызванные заболеванием) переломы костей. Из-за недостаточного количества нормальных зрелых лейкоцитов возможны частые инфекции. Повышение температуры может наблюдаться как в связи с возникшей на фоне лейкоза инфекцией, так и из-за опухолевой интоксикации. Иногда одним из проявлений острого лейкоза является продолжительная ангина, плохо поддающаяся терапии антибиотиками.
В некоторых случаях ОЛЛ вызывает изменения и в других органах: глазах, почках, яичках у мальчиков и яичниках у девочек, причем у мальчиков поражение половых органов наблюдается чаще. Нередко возникает поражение центральной нервной системы — нейролейкемия.
Так как все наблюдаемые симптомы могут быть связаны и с другими заболеваниями и не специфичны для ОЛЛ, перед началом лечения необходима лабораторная диагностика, которая в срочном порядке производится в больничных условиях.
Когда идут в олл-ин
Намерений сделать такую «финишную» ставку может быть несколько:
1
Покерист пытается выбить оппонентов из раздачи совершив большую ставку. Такое действие может совершаться как блефом, так и с наличием неплохой комбинации на руках. В первом случае есть вероятность того, что какой-либо из соперников останется в раздаче и выиграет ее. Во втором случае, даже если кто-то остался, есть шанс его переиграть.
2
Вынудить противника поставить весь стек. Только такой кардинальной ставкой можно заработать сразу много.
3
Игрок играет исключительно в агрессивном стиле. Для него All-in характерное явление – даже без сильных комбинаций на руках.
4
У участника сильная комбинация на руках и он ставит все в уверенности что получит весь банк. Однако опытные игроки не советуют делать этого даже со стритом, флэшем или фулл-хаусом.
5
Попытка кражи блайндов. В таких случаях редко используется all–in, но иногда возникают такие ситуации. Обычно для кражи блайндов в покере сильно рейзят в начале игры, выбивая оппонентов из раздач до флопа.
6
Во время турниров олл-ин делают в тех случаях, когда игрок продолжительное время проигрывает на блайдах и у него остается количество фишек кратное 10 большим блайндам. В таком случае олл-ин может спасти ситуацию, не заставляя игрока дожидаться медленного проигрыша.
Получить бонус